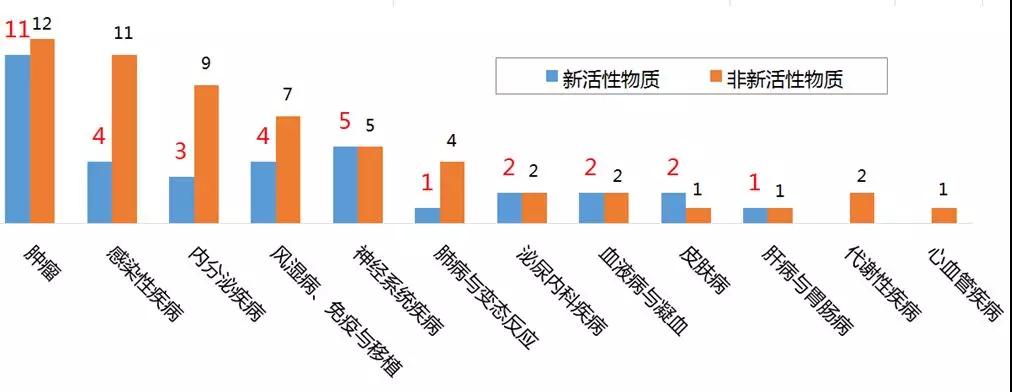
推荐上市的药物中,51个药物是增加新的适应症,35个是以前从未在欧盟批准过的新活性物质(new active substance, NAS),2个先进治疗产品(advanced therapy medicinal products, ATMPs),19个孤儿药;7个药物获得加快评估(accelerated assessments),3个药物获得条件上市许可(conditional marketing authoristations),2个药物获得特殊情况批准(approval under exceptional circumstances)。这些药物中有许多显著改善了相关疾病的治疗。按治疗领域的具体分类情况见图1。
图1 2017年EMA推荐上市的药物数量(按治疗领域分类)
9个改善疾病治疗药物
包括4个儿科药、2个先进治疗产品、3个孤儿药
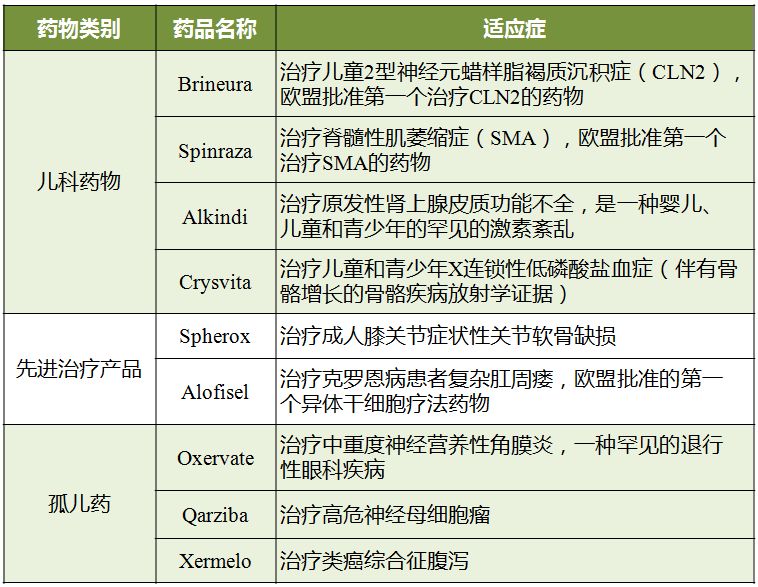
2017年EMA推荐上市了一批显著改善相关疾病治疗的药物(具体情况见表1)。对于公共健康来说,药品上市许可的发展是必不可少的,更在于其具有改善疾病治疗的潜力。
EMA致力于确保开展儿科药物的伦理研究和进行适时的上市许可,2017年是欧盟儿科药物法规(No 1901/2006/EC)实施的第十年,该法规旨在促进优质、安全和有效的儿科药物的研发。ATMPs(先进治疗产品)则是以基因或细胞为基础的药物,给疾病治疗提供新的、突破性的机会。它们对于严重的、无法治愈的或传统方法无法根治的慢性疾病尤为重要。欧盟的孤儿药政策法规体系旨在通过给研发者提供激励,以促进该类药物的研发和上市许可。
表1 2017年EMA推荐上市的显著改善相关疾病治疗的药物
12个优先推荐上市药物
包括7个加快评估、3个条件上市许可、2个特殊情况批准
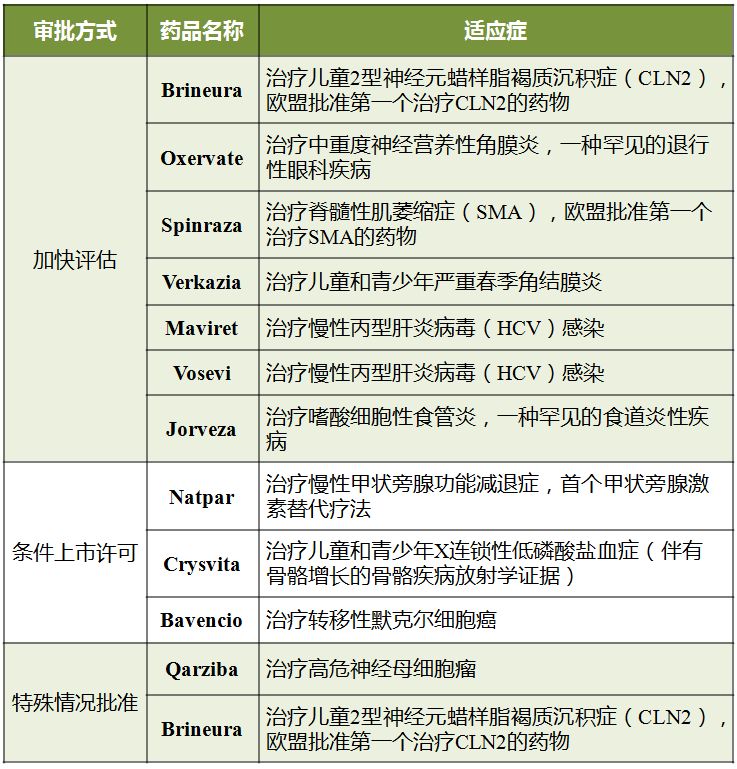
欧盟药物立法包括相关若干条款,以促进患者更早获得满足公共卫生需要的和进入集中审批程序(centralised procedure)的新药。如:加速评估、条件上市许可与特殊情况批准等。2017年,EMA优先推荐上市的药物数量为12个。(具体情况见表2)。
表2 2017年EMA优先推荐上市的药物
其中,7个药物在加速评估条件下获得推荐上市许可。这一机制是专为能够满足未满足的医疗需求的药物而制定的,它允许EMA的科学委员会更快地对相应药物进行评估(在150天之内,而不是210天内)。
3个药物获得条件上市许可,这是欧盟允许患者尽早获得新药的手段之一。如果药物能够解决紧急的、未满足的医疗需求,这一机制则允许在不完全的临床数据的基础上尽早批准一种药物,而不是通常情况下需要的全部临床数据。这些药物的研发者必须履行药品上市许可后的法定义务,以获得关于药物的完整数据。
2个药物获得特殊情况批准,当完整的数据无法获得时,这一路径允许患者获得正常上市许可条件下不可能批准的药物。原因在于某一疾病只有很少的患者,或获得完整的药物疗效和安全性的信息是不道德的,或目前尚存科学知识方面的空白。这些药物上市许可后必须接受专门的药物警戒和监督。
 客服热线:
客服热线: