CFDA发布了《国家医疗器械质量公告(2017年第26期,总第44期)》,又有11款医疗器械产品不符合标准规定。
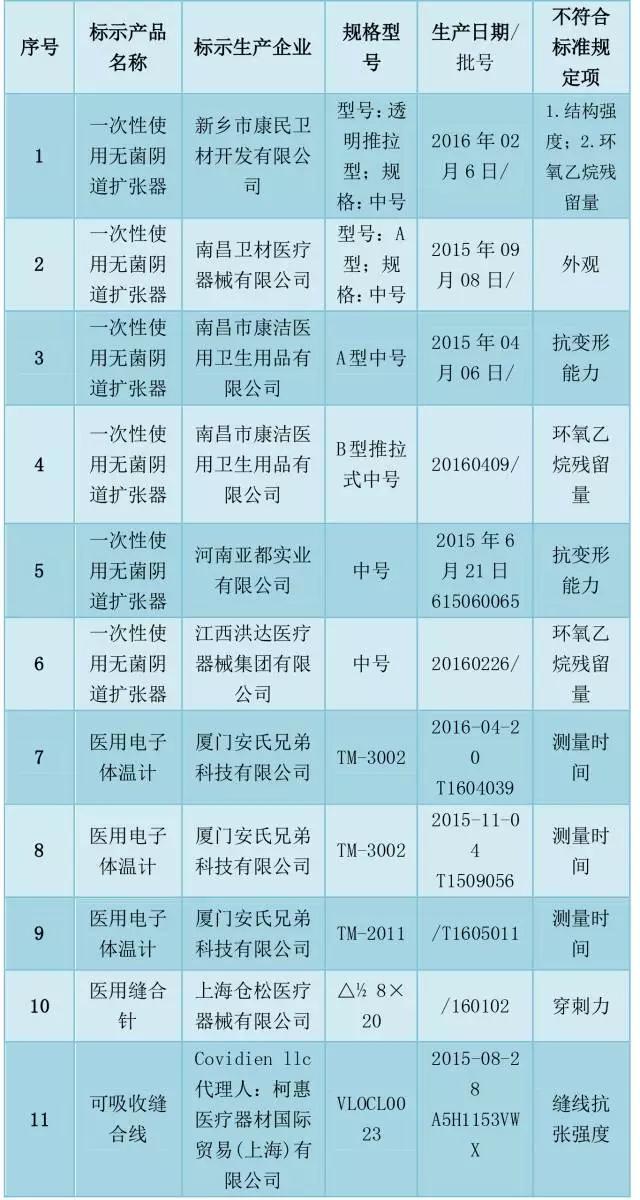
此次被抽检项目不符合标准规定的医疗器械产品,涉及8家企业的3个品种11批(台)。具体为:
一次性使用无菌阴道扩张器5家企业6批次产品。
新乡市康民卫材开发有限公司生产的1批次一次性使用无菌阴道扩张器,结构强度、环氧乙烷残留量不符合标准规定;
南昌卫材医疗器械有限公司生产的1批次一次性使用无菌阴道扩张器,外观不符合标准规定;
南昌市康洁医用卫生用品有限公司生产的2批次一次性使用无菌阴道扩张器,1批次抗变形能力、1批次环氧乙烷残留量不符合标准规定;
河南亚都实业有限公司生产的1批次一次性使用无菌阴道扩张器,抗变形能力不符合标准规定;
江西洪达医疗器械集团有限公司生产的1批次一次性使用无菌阴道扩张器,环氧乙烷残留量不符合标准规定。
医用电子体温计1家企业3台产品。厦门安氏兄弟科技有限公司生产的3台医用电子体温计,测量时间不符合标准规定。
医用缝合针(线)2家2批次产品。上海仓松医疗器械有限公司生产的1批次医用缝合针,穿刺力不符合标准规定;
Covidien llc生产的1批次可吸收缝合线[代理人:柯惠医疗器材国际贸易(上海)有限公司],缝线抗张强度不符合标准规定。
对上述抽检中发现的不符合标准规定产品,食药总局已要求企业所在地省级食药监部门对相关企业进行调查处理,监督企业进行产品召回、不合格原因调查、整改措施及公开披露信息的落实情况;产品对人体造成伤害或者有证据证明可能危害人体健康的,应依法采取暂停生产、经营、使用的紧急控制措施;需要暂停进口的,应及时报总局做出行政处理决定。
 客服热线:
客服热线: