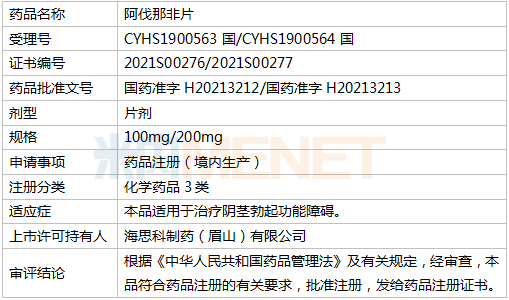
药品相关情况
资料显示,阿伐那非片最初由日本田边三菱制药株式会社授权美国VIVUS公司开发的用于治疗男性勃起功能障碍的药物,2012年4月在美国上市,商品名为Stendra。2013年6月被批准在欧盟上市,商品名为Spedra。目前已在美国、德国、法国、意大利等多国上市,在国内尚无生产和进口,海思科开发的阿伐那非片是国内首家仿制。
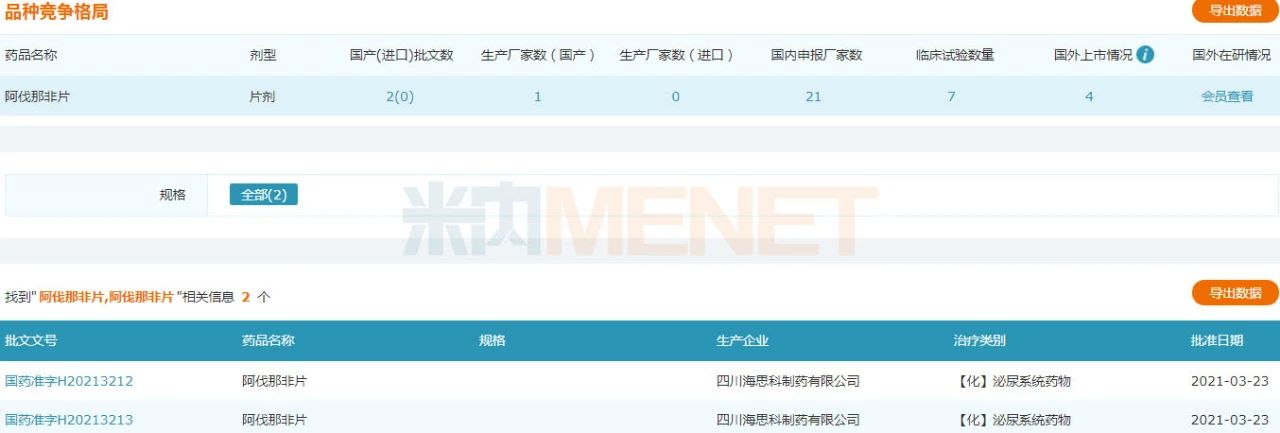
来源:米内网一键检索
阿伐那非片为海思科开发的仿制药产品,该产品在2016年8月获国家药监局颁发《药物临床试验批件》,在完成BE研究和Ⅲ期临床研究后,2019年7月递交了上市申请。米内网数据显示,2019年中国城市公立医院、县级公立医院、城市社区中心以及乡镇卫生院(简称中国公立医疗机构)及中国城市实体药店终端抗ED药物市场规模超过33亿元。
同日,海思科还发布公告称,海思科医药集团股份有限公司创新药HSK21542注射液用于腹部腔镜手术术后镇痛的Ⅲ期临床试验方案于近日获CDE同意,可开始实施Ⅲ期临床试验的受试者入组用药等工作。

药品基本情况
HSK21542是由海思科自主研发,具有完全自主知识产权的新分子实体化合物,属于强效外周Kappa受体激动剂,拟用于镇痛、慢性肾脏疾病相关性瘙痒(CKD-aP)的治疗等。截至公告披露日,全球尚未有获批上市的同类化合物,目前同类化合物研发进度最领先的为Cara Therapeutics Inc.(NASDAQ:CARA)开发的KORSUVA(CR845/difelikefalin)。
HSK21542于2019年10月-2020年10月在澳洲开展了I期临床试验;2020年1月-2020年9月在中国开展了I期临床试验;2020年6月-2021年2月在中国开展了用于腹部腔镜手术术后镇痛的Ⅱ期临床试验。根据前期临床试验数据结果,公司做出该项目进入Ⅲ期临床试验的决定。除上述适应症和临床试验外,HSK21542目前还在开展在血液透析受试者中的Ⅱ期临床试验。




