而研发驱动型小公司在今年也都开始进入到重要阶段,其中歌礼药业新药刚刚宣布上市。而百济神州、信达生物等均有重磅品种在中国/美国正在进行三期临床。
显然,一个蓬勃发展的创新药时代正在向中国医药行业走来。对于身处与医药产业的每一个人而言,企业选择怎样的未来,就是医药行业的未来。从长远来看,以营销为主要竞争力,主打“神药”的企业终究是没有前途的,但如果按照“女怕嫁错郎,男怕入错行”的逻辑,无论是职业经理人,还是普通人员,选择一个真正有实力的企业,才是赢得未来的关键。
那么,在下一个时间,谁会在创新的赛道上胜出?谁家的储备产品最具有实力?
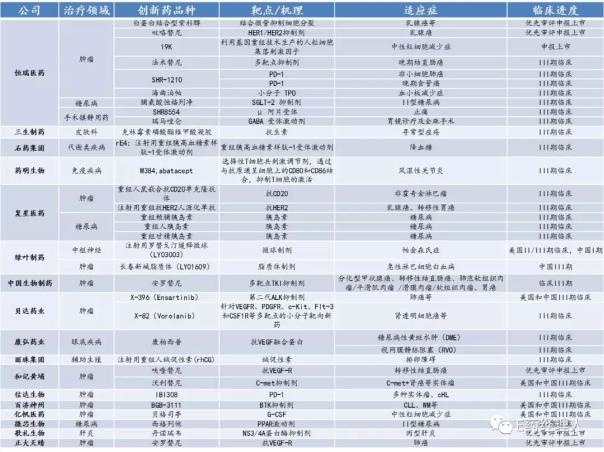
来源:药智网,兴业证券经济与金融研究院整理
恒瑞医药
说起医药创新,恒瑞是绕不开的存在。截止2018年5月公司共有7种产品处于三期临床阶段,包括治疗肿瘤的法米替尼、SHR-1210、海曲泊帕;治疗糖尿病的脯氨酸恒格列净;和手术镇静用药SHR8554、甲苯磺酸瑞马唑仑。
法米替尼是恒瑞医药自主研发且具有知识产权的化学类抗肿瘤新药,是一个口服多靶点受体酪氨酸激酶抑制剂。法米替尼具有抗增殖和抑制血管生成的双重抗肿瘤作用。此产品最早于2008年6月申报临床,历经发补,是一个多靶点小分子靶向药物。目前临床前药效研究发现法米替尼对多种靶点酪氨酸激酶均有明显的抑制作用。
葛兰素史克公司研发的非肽类 TPO激动剂艾曲泊帕(Eltrombopag,PROMACTA)于 2008 年 11 月 20 日获美国 FDA 批准上市。虽然艾曲泊帕优势明显,但副作用依然存在。艾曲泊帕最常见的严重不良反应是出血,且绝大多数出血反应都发生于停药后。另外艾曲泊帕易引起肝脏毒性、肝脏损伤和骨髓纤维化。因此为了寻找更加高效、低毒的 TPO 激动剂,对艾曲泊帕进行了一系列结构的修饰,研究开发具有自主知识产权的高选择性 TPOR 激动剂海曲泊帕。
恒格列净是恒瑞自主研发的1.1类新药,属于SGLT-2(钠-葡萄糖转运蛋白2)抑制剂。SGLT2抑制剂可抑制肾脏对葡萄糖的重吸收,增加尿中的排糖量,从而调节体内的血糖平衡。该机制有别于目前已有的降糖方式,故理论上无低血糖和增加体重的风险。基于这个特性,SGLT2抑制剂已成为糖尿病药物研发中的一大热点。恒瑞最早在2012年2月9日向江苏省食品药品监督管理局提交了恒格列净的临床申请,在2012年4月20日获得CDE承办受理,2013年4月11日获批临床。恒瑞医药在2016年10月提交了恒格列净的补充申请,并在2017年3月获批开展II期、III期临床试验。
SHR8554 注射液是一种靶向 μ 阿片受体(MOR) 的小分子药物,可激活 MOR 受体,适用于疼痛的治疗。 由恒瑞医药、江苏盛迪、成都盛迪和上海恒瑞共同开发研制且具有自主知识产权,目前国外在研的同类产品为 Trevena 公司开发的 Oliceridine(TRV130),该产品目前在美国处于 III 期临床研究阶段。目前我国尚无同类药处于临床研究阶段或者上市。预计上市后讲会填补我国在这片领域的空白。
2017年6月9日,恒瑞宣布旗下创新药甲苯磺酸瑞马唑仑获得CFDA批准,成功挺进Ⅲ期临床,顺利的话,该药有望在近两年上市,甲苯磺酸瑞马唑仑是恒瑞的1.1类新药,用于患者的静脉麻醉,并且适应症可扩展至镜检时镇痛、术前麻醉和ICU镇静。甲苯磺酸瑞马唑仑疗效和安全性有望优于咪达唑仑和异丙酚。根据数据,国内咪达唑仑市场约2亿元,异丙酚市场约23亿元。苯磺酸瑞马唑仑如果获批上市,有望凭借其竞争优势强占市场,潜力超过10亿元。
石药集团
石药集团的rE4属于GLP-1类似物,是生物1类创新药,目前处于临床三期,预计2019年获批,该产品主要用于糖尿病降低血糖。目前市场上的同类产品可对标药物诺和诺德的诺和力(利拉鲁肽),于2009年上市,2015年全球销售额20.7亿美元,目前同比仍保持18%的增速在增长,预计rE4上市后能够对其产生一定的冲击,抢占部分市场份额。
绿叶制药
绿叶制药目前共有两款产品进入了三期临床,分别是治疗中枢神经领域的注射用罗替戈汀缓微球(LY03003)和适应于肿瘤领域的长春新碱酯质体。
其中注射用罗替戈汀缓微球(LY03003)为绿叶制药长效缓释制剂平台开发的重点中枢神经系统在研产品之一,采用一周一次肌肉注射给药,是全球首个长期产生持续多巴胺受体刺激素(Continuous Dopamine Stimulation)的产品。该药物在人体内的稳定释放能够减轻帕金逊患者药物治疗易出现的?开关?效应,显着改善晚期帕金逊病患者易出现的运动并发症,长期应用有望推迟运动并发症的产生。目前该药物在美国、中国、欧洲和日本市场进行同步开发;而治疗急性淋巴细胞白血病、淋巴瘤的硫酸长春新碱脂质体现在也处于临床三期阶段,根据预测,目前中国的潜在市场规模约为603亿,预计正式上市后,会占有相当大的利润。
复星医药
复星医药目前有五种产品正在进入三期临床,包括位于肿瘤领域的重组人鼠嵌合CD20单克隆抗体和注射用重组抗HER2人源化单抗;位于糖尿病领域的重组赖脯胰岛素、重组人胰岛素以及重组甘精胰岛素。
其中,重组人鼠嵌合CD20单克隆抗体主要适用于非霍奇金淋巴瘤、类风湿性关节炎的治疗,和鼠源单抗、嵌合单抗、人源化单抗相比,全人源单抗的重链和轻链均来源于人,因此副作用更小,免疫亲和力基本保持不变,被称为未来的主流技术。目前国际已经获批生产的全人源化单抗药不到10个,其中雅培的阿达木单抗(humira)是疗效最好的产品,其2012年全球销售额约为95亿美元。而重组抗HER2人源化单抗是于2016年1月获得国家食药监总局的临床试验批准。该产品用于转移性胃癌适应症和乳腺癌等症,目前针对该产品已投入研发费用人民币约2.29亿元。
位于糖尿病领域的重组赖脯胰岛素为第三代胰岛素产品,与人胰岛素分子序列极为接近,相比普通胰岛素,它的起效时间提前约25-30分钟,提高了病人的依从性,可有效控制餐后血糖;且该药具有速效作用,消除快,可以有效回避迟发性餐后低血糖,控制低血糖。
贝达药业
贝达药业目前在研的产品有位于肿瘤治疗领域的X-396(Ensartinib)和X-82(Vorolanib)两款产品进入了三期临床。
其中X-396(Ensartinib)由贝达药业控股子公司美国Xcovery Holding Company LLC开发。作为肺癌治疗的新一代ALK抑制剂,X-396具有抗ALK的活性,用于治疗有ALK突变的肺癌患者。X-39对于ALK阳性肺癌细胞系的抑制能力,是目前作为肺癌一线治疗药物的10倍,不仅如此,对于导致克唑替尼耐药的L1196M和C1156Y突变,X-396也表现出较强的抑制活性。
而X-82(Vorolanib)化合物,是一款针对血管内皮生长因子受体(VEGFR)和血小板衍化生长因子受体(PDGFR)靶点的口服抑制剂,可用于眼科及肾癌、胃癌、肺癌等多种癌症的治疗。
和记黄埔
和记黄埔目前在研的产品有位于肿瘤领域的沃利替尼进入了三期临床,沃利替尼是和记黄埔医药(上海)有限公司自主研发的一种强效、高选择性小分子c-Met激酶抑制剂,为沃利替尼通过抑制作用于人体一种叫做c-Met的激酶来阻断肿瘤细胞的生长,并阻止其转移到身体其它部分。
沃利替尼在细胞和动物试验中已显示能抑制肿瘤细胞的生长。目前在动物试验中也显示出较好的安全性,预计该产品上市后能够为晚期肺癌患者提供了可能的新的治疗选择。
信达生物
信达生物目前在研的产品有位于肿瘤领域的IB308进入了三期临床。IBI308是信达生物开发的抗PD-1单克隆抗体注射液,通过阻断体内PD-1与配体PD-L1之间的结合,使T细胞发挥正常作用,进而利用自身免疫将肿瘤细胞消灭。IBI308进入三期临床。使信达成为恒瑞之后国内第2家进入III期临床的PD-1/PD-L1药物开发企业。
百济神州
百济神州目前在研的产品有位于肿瘤领域的BGB-3111进入了三期临床。GB-3111是百济神州开发的高选择性BTK抑制剂,之前公布的单药治疗多种晚期B细胞恶性肿瘤的I期研究显示,BGB-3111对慢性淋巴细胞白血病的总应答率高达93%,对套细胞淋巴瘤的应答率达到80%,而依鲁替尼对于这两个适应症的应答率分别为66%和43%,提示BGB-3111可能会比依鲁替尼有更好的疗效。预计上市之后会对依鲁替尼得市场份额产生不小的影响。
亿帆医药
亿帆医药目前在研的产品有位于肿瘤领域的贝格司亭进入了三期临床。贝格司亭属于第三代长效G-CSF,与第一代和第二代相比,双分子结构使其有可能解决肿瘤病人化疗后发生重度嗜中性粒细胞减少症的医学难题,具有成为最佳重组人G-CSF药物的潜力。贝格司亭直接对标安进的Neulasta,在保证质量与疗效与原研相同的前提下,在产品剂量、用药便利性及价格等方面具有一定的优势。业界观点认为,作为创新型长效升白药,贝格司亭也在技术和质量上领先恒瑞的19K。
Neulasta的全球销售额在46亿美元以上,全球G-CSF的市场规模大概为66亿美元,根据第三方机构预测,贝格司亭有望获得10亿美元的市场规模。
2018年,是中国改革开放40周年。在过去的40年里,“中国制造”席卷全球,但唯独医药制剂产品发展迟缓,在国际市场迟迟打不开局面,收获不了认可。现在这个节点,中国加入ICH,各种标准与监管政策向国际标准看齐,而国内则一批创新药(国家定义“全球新”)正在进入最后的冲刺阶段,那么从现在瞄准全球,“从这里瞄准世界”!中国药企会不会在下个十年收获全世界的认可?
未来十年到底如何,我们需要探究,我们需要站在巨人的肩膀上看清医药界的未来。9月1日,由中国医药企业管理协会、中国医药生物技术协会主办,中国农工民主党中央医疗卫生·生物技术工作委员会指导的第十届中国医药企业家科学家投资家大会暨改革开放四十年医药企业创新成果展将于2018 年9月1日~3日在北京雁栖湖举行。届时将会有1000+创新项目、200+临床专家、500+投资家、500+科学家、500+企业家、200+媒体总编参与,共同见证中国医药创新的崛起,也共同探讨,中国医药创新如何走向世界!




